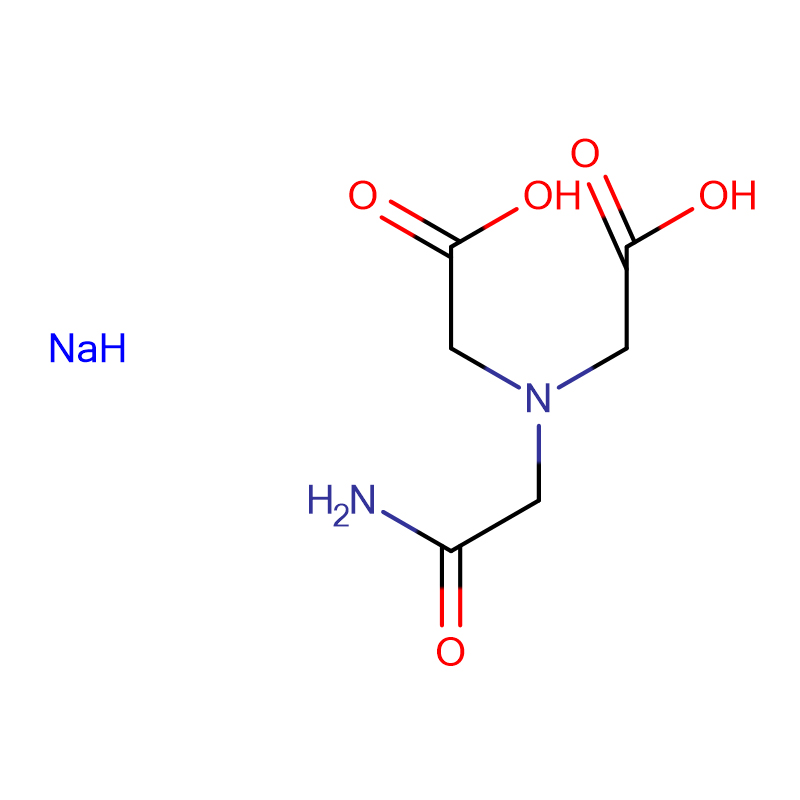
ADA DISODIUM SOUT Cas:41689-31-0 N- (2- Amino- 2- oksoetiel)- N- (karboksimetiel) glisiennatriumsout Wit kristallyne poeier 98%
| Katalogusnommer | XD90092 |
| Produk Naam | ADA DINATRIUM SOUT |
| CAS | 41689-31-0 |
| Molekulêre Formule | H2NCOCH2N(CH2CO2Na)2 |
| Molekulêre gewig | 234,12 |
| Berging besonderhede | Omgewing |
| Geharmoniseerde Tariefkode | 292419009 |
Produk spesifikasie
| Voorkoms | Wit kristallyne poeier |
| Assay | >98.0% |
| Berging Temp | Stoor by RT |
Buffer is 'n oplossing wat pH-veranderinge kan weerstaan wanneer 'n klein hoeveelheid suur of alkali en water bygevoeg word.Die pH-bufferstelsel speel 'n belangrike rol in die handhawing van die normale pH-waarde van organismes en die normale fisiologiese omgewing.Die meeste selle kan slegs in 'n baie nou pH-reeks werk.Dit moet 'n bufferstelsel hê om die pH-veranderinge wat tydens metabolisme plaasvind te weerstaan.Daar is drie hoof pH-bufferstelsels in die organisme, dit is proteïen- en bikarbonaatbufferstelsels.Die hoeveelheid van elke bufferstelsel Dit verskil in verskeie tipes selle en organe.
Die buffer-effek van die bufferoplossing wat uit die swak suur HA en sy sout NaA saamgestel is op die suur is as gevolg van die teenwoordigheid van 'n voldoende hoeveelheid alkali A- in die oplossing.Wanneer 'n sekere hoeveelheid sterk suur by hierdie oplossing gevoeg word, word H-ione hoofsaaklik deur A-ione verbruik:
Daarom is die pH-waarde van die oplossing byna onveranderd;wanneer 'n sekere hoeveelheid sterk basis bygevoeg word, verbruik die swak suur HA in die oplossing OH-ione en belemmer die verandering van pH.
Voeg 'n klein hoeveelheid sterk suur of sterk basis by die bufferoplossing, die pH-waarde van die oplossing sal nie veel verander nie, maar as die hoeveelheid suur of alkali bygevoeg word, sal die bufferoplossing sy buffer-effek verloor.Dit wys dat sy bufferkapasiteit 'n sekere limiet het.
Die bufferkapasiteit van 'n bufferoplossing hou verband met die konsentrasie van die komponente waaruit die bufferoplossing bestaan.Die bufferoplossing wat bestaan uit 0.1mol·L-1HAc en 0.1mol·L-1NaAc het 'n groter bufferkapasiteit as die bufferoplossing van 0.01mol·L-1HAc en 0.01mol·L-1NaAc.Dit kan deur berekening bevestig word.Die konsentrasie van die komponente van die bufferoplossing moet egter nie te groot wees nie, anders kan die interaksie tussen die ione nie geïgnoreer word nie.