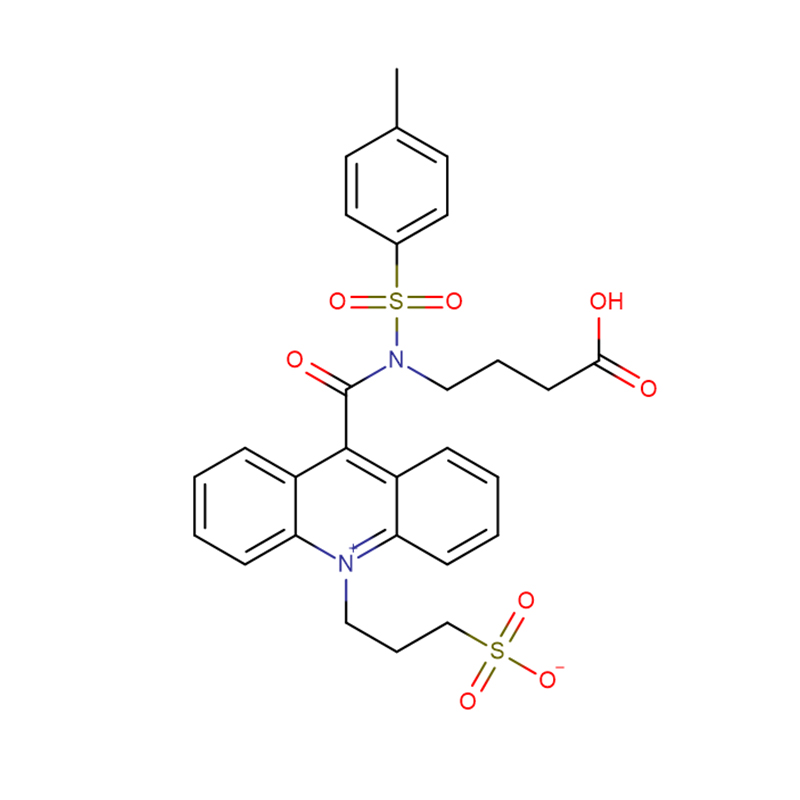
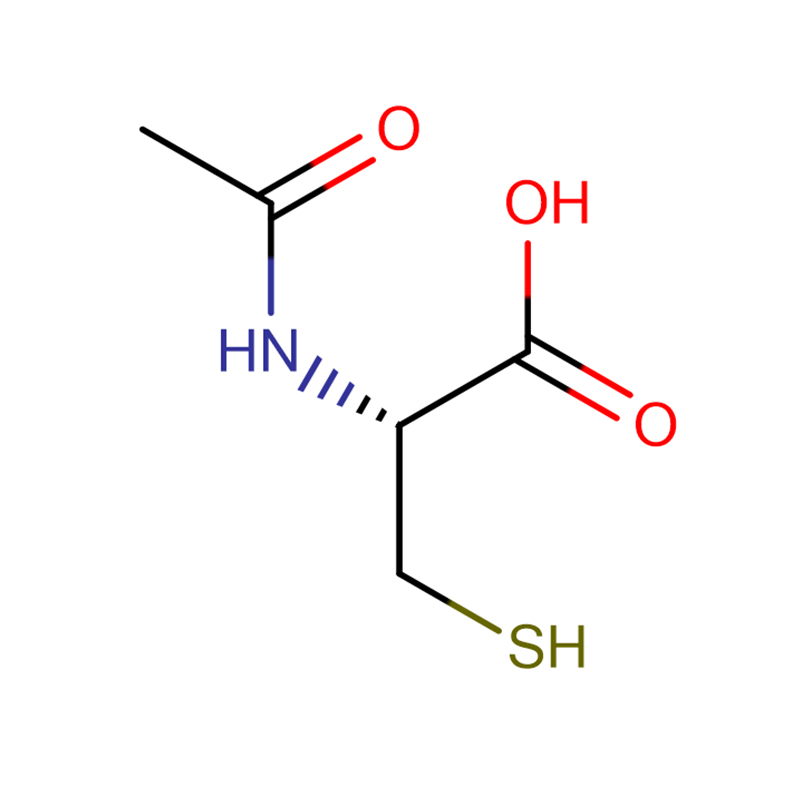
4-Amino-3-hidrasino-1,2,4-triasool-5-tiol Cas:28836-03-5 99% Geel tot groen vaste stof
| Katalogusnommer | XD90146 |
| Produk Naam | 4-Amino-3-hidrasino-1,2,4-triasool-5-tiol |
| CAS | 28836-03-5 |
| Molekulêre Formule | C16H13NO3S·NH3 |
| Molekulêre gewig | 316,37 |
| Berging besonderhede | Omgewing |
| Geharmoniseerde Tariefkode | 2923900090 |
Produk spesifikasie
| Voorkoms | Geel tot groen soliede |
| Assay | ≥ 99% |
| Smeltpunt | 237°C(onts.)(lit.) |
| Oplosbaarheid | NaOH: oplosbare 1 N |
| Wateroplosbare | Oplosbaar in water, 1N NaOH en metanol. |
1.Ons het die inhiberende effekte van isorhamnetin op sampioen-tyrosinase bestudeer deur inhibisiekinetika en berekeningsimulasie.Isorhamnetin het tyrosinase omkeerbaar geïnhibeer op 'n gemengde-tipe wyse by Ki=0.235±0.013 mM.Metings van intrinsieke en 1-anilinonaftaleen-8-sulfonaat(ANS)-bindende fluoressensie het getoon dat isorhamnetien nie betekenisvolle veranderinge in die tersiêre struktuur van tyrosinase veroorsaak het nie.Om insig in die inaktiveringsproses te kry, is die kinetika bereken deur middel van tyd-intervalmetings en deurlopende substraatreaksies.Die resultate het aangedui dat inaktivering geïnduseer deur isorhamnetin 'n eerste-orde reaksie met bifasiese prosesse was.Om verdere insig te verkry, het ons koppeling tussen tyrosinase en isorhamnetien gesimuleer.Simulasie was suksesvol (bindingsenergieë vir Dock6.3: -32.58 kcal/mol, vir AutoDock4.2: -5.66 kcal/mol, en vir Fred2.2: -48.86 kcal/mol), wat daarop dui dat isorhamnetien met verskeie residue in wisselwerking tree, bv. as HIS244 en MET280.Hierdie strategie van voorspelling van tyrosinase-interaksie in kombinasie met kinetika gebaseer op 'n flavanoonverbinding kan nuttig wees in sifting vir potensiële natuurlike tyrosinase-inhibeerders.
2. Suur ontvouende pad van konalbumien (CA), 'n monomere glikoproteïen van hoender eierwit, is ondersoek met behulp van ver- en naby-UV CD spektroskopie, intrinsieke fluoressensie emissie, ekstrinsieke fluoressensie sonde 1-anilino-8-naftaleen sulfonaat (ANS) en dinamiese ligverstrooiing (DLS).Ons neem pH-afhanklike veranderinge in sekondêre en tersiêre struktuur van CA waar.Dit het inheemse α-helikale sekondêre struktuur by pH 4.0 maar verliesstruktuur by pH 3.0.Die CA het uitsluitlik bestaan as 'n pre-gesmelte globule toestand en gesmelte globule toestand in oplossing by pH 4.0 en pH 3.0, onderskeidelik.Die effek van pH op die konformasie en termostabiliteit van CA wys na sy hittebestandheid by neutrale pH.DLS resultate toon dat MG toestand as kompakte vorm bestaan het in waterige oplossings met hidrodinamiese radiusse van 4.7 nm.Uitblus van triptofaanfluoressensie deur akrilamied het verder die ophoping van 'n intermediêre toestand, gedeeltelik ontvou, tussen inheemse en ontvoude toestande bevestig.


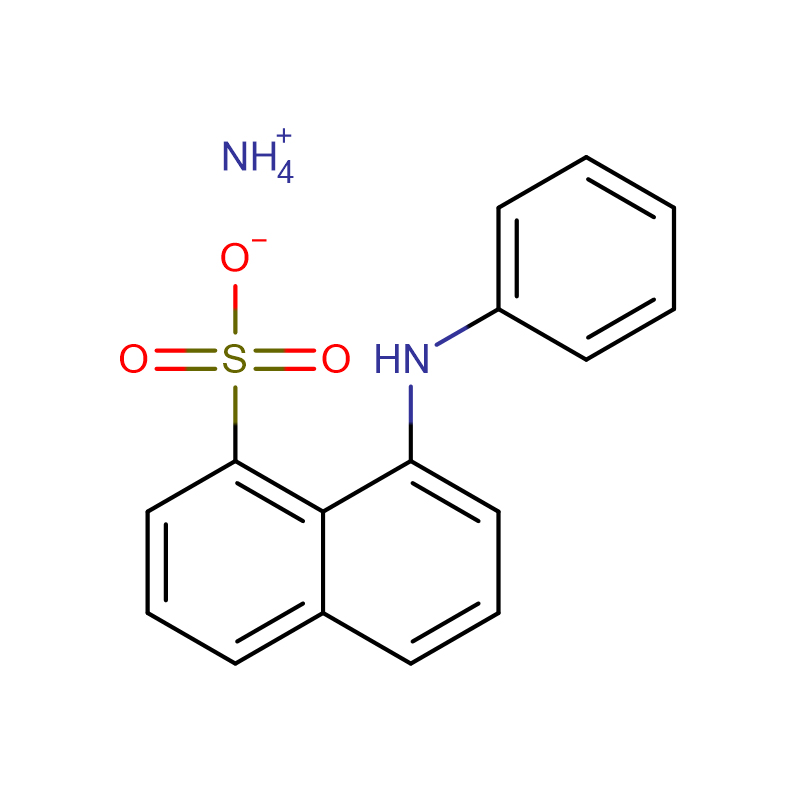


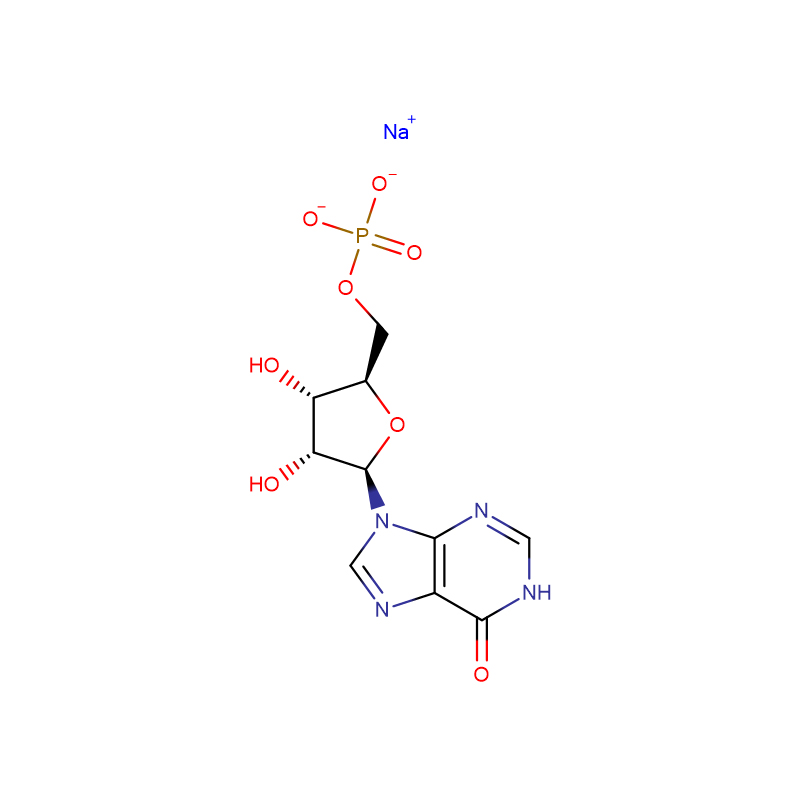
![N-[[bis[4-(dimetielamino)feniel]amino]karboniel]glisiennatriumsout Wit tot grysgroen kristallyne poeier](http://cdn.globalso.com/xdbiochems/115871-19-7.jpg)